|
Реальные газы отличаются от идеальных тем, что молекулы этих газов имеют конечные собственные объемы и связаны между собой сложными силами взаимодействия. При высоких давлениях и достаточно низких температурах реальные газы конденсируются, т. е. переходят в жидкое состояние, чего принципиально не может быть с идеальными газами.
В 1861 году ирландский физик-химик Т. Эндрюс экспериментально исследовал зависимость давления углекислого газа от объема при изотермическом сжатии. На рис. 1 схематично представлены результаты опытов, подобных опытам Т. Эндрюса. Рассмотрим изотерму АВСD.
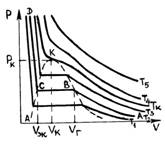 |
| рис. 1 |
На участке АВ уменьшение объема, занятого газом, сопровождается увеличением давления сначала обратно пропорционально объему, затем все медленнее.
В точке В начинается конденсация газа и продолжается при постоянном давлении, называемом давлением насыщенных паров, до точки С. В точке С процесс конденсации газа заканчивается, при дальнейшем уме-ньшении объема осуществляется сжатие жидкости (участок СD), сопровождающееся быстрым ростом давления, свидетельствующее о том, что жидкость слабо сжимаема. При уменьшении давления, действующего на жидкость, вещество пройдет те же состояния в обратном порядке: оно расширится по пути DС до точки кипения, произойдет испарение (путь СВ), а затем получившийся пар расширится до исходного давления (точка А).
На участке ВС не только давление, но и температура постоянны. Крайним точкам отрезка ВС соответствуют однофазные состояния вещества: точке С (объем 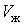 ) – жидкое, а точке В (объем ) – жидкое, а точке В (объем 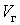 ) – газообразное. В промежуточном двухфазном состоянии с объемом V часть вещества с количеством молей ) – газообразное. В промежуточном двухфазном состоянии с объемом V часть вещества с количеством молей 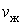 находится в жидком, а часть с количеством молей находится в жидком, а часть с количеством молей 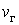 – в газообразном состоянии. Определим отношение количества молей жидкой и газообразной фаз в объеме V . – в газообразном состоянии. Определим отношение количества молей жидкой и газообразной фаз в объеме V .
Объем одного моля жидкой и газообразной фаз вещества соответственно равны:
|
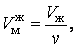 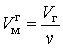 |
(5.1.1) |
Объем V содержит 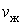 молей жидкой фазы и молей жидкой фазы и 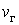 молей газообразной фазы, поэтому этот объем можно представить в виде суммы объемов жидкой и газообразной фаз следующим образом: молей газообразной фазы, поэтому этот объем можно представить в виде суммы объемов жидкой и газообразной фаз следующим образом:
|
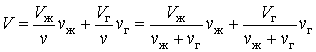 |
(5.1.2) |
После простых преобразований из выражения (5.1.2) находим искомое отношение
|
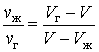 |
(5.1.3) |
Умножая числитель и знаменатель левой части выражения (5.1.3) на молярную массу вещества, получим аналогичное отношение для масс жидкой и газообразной фаз:
|
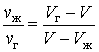 |
(5.1.4) |
На рис. 1 представлены изотермы газа при различных температурах 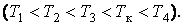 Из рисунка видно, что с ростом температуры горизонтальный участок, соответствующий двухфазному состоянию вещества, уменьшается и при некоторой температуре Из рисунка видно, что с ростом температуры горизонтальный участок, соответствующий двухфазному состоянию вещества, уменьшается и при некоторой температуре 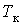 , называемой критической, стягивается в точку K . Изотерма, соответствующая температуре , называемой критической, стягивается в точку K . Изотерма, соответствующая температуре 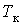 , называется критической изотермой, точка K которой является точкой перегиба. , называется критической изотермой, точка K которой является точкой перегиба.
| 
